Table of Contents
Toggle1. রাসায়নিক গণনা MCQ
রাসায়নিক গণনা - প্রশ্ন উত্তর MCQ
1.1 49 গ্রাম H2SO4 কে সম্পূর্ণ প্রশমিত করতে কত গ্রাম NaOH প্রয়োজন? a) 40 গ্রাম b) 4 গ্রাম c) 80 গ্রাম d) 8 গ্রাম
সঠিক উত্তর-a) 40 গ্রাম
ব্যাখ্যা- বিক্রিয়ার সমীকরণঃ 2NaOH+H2SO4 → Na2SO4 + 2H2O
1 মোল H2SO4= (2×1+32+4×16) গ্রাম= 98 গ্রাম
2 মোল NaOH= 2(23+16+1) গ্রাম= 80 গ্রাম
∴ 49 গ্রাম H2SO4 কে সম্পূর্ণ প্রশমিত করতে NaOH-এর পরিমাণ =\frac{49\times 80}{98} গ্রাম=40 গ্রাম
1.2 12g কার্বনের সঙ্গে 32g অক্সিজেনের বিক্রিয়ায় কত মোল কার্বন ডাই অক্সাইড উৎপন্ন হবে? a) 1 b) 2 c) 0.5 d) 4.4
সঠিক উত্তর- a) 1mol CO2 ব্যাখ্যা- C+O2→ CO2; 1mol CO2= (12+16×2)g =44g
1.3 ক্যালসিয়াম কার্বনেটে ক্যালসিয়ামের শতকরা পরিমাণ a)50% b)20% c) 10% d) 40%
সঠিক উত্তর- d)40%
ব্যাখ্যা- 1 গ্রাম অনু ক্যালসিয়াম কার্বনেট (CaCO3) = (40+12+3×16)g = 100g। Ca এর শতকরা পরিমাণ= \frac{40}{100}×100%=40%
1.4 40 gm NaOH -কে সম্পূর্ণ প্রশমিত করতে কত gm H2SO4 প্রয়োজন? (a) 40 gm (b) 4gm (c)49gm (d) 8 gm
সঠিক উত্তর- (c)49gm
ব্যাখ্যা- বিক্রিয়ার সমীকরণ- 2NaOH+H2SO4→2H2O+Na2SO4।
সুতরাং 2 mol NaOH =2 (23+16+1) gm = 80 gm । 1mol H2SO4= (1×2+32+16×4) gm = 98 gm
80 gm NaOH কে প্রশমিত করে 98 gm H2SO4
1 gm NaOH কে প্রশমিত করে \frac{98}{80} gm H2SO4
40 gm NaOH কে প্রশমিত করে \frac{98\times40}{80} gm H2SO4= 49 gm
1.5 কার্বনযুক্ত কোন গ্যাসীয় পদার্থের বাষ্প ঘনত্ব 13 হলে, তার আণবিক সংকেত নিচের কোনটি হতে পারে? a) CO2 b) C2H4 c) C2H6 d) C2H2
বাষ্প ঘনত্ব =13 । আণবিক গুরুত্ব =2×13=26
এখন, CO2= 12+16×2=44; C2H4=12×2+1×4=28 ; C2H6=12×2+1×6=30; C2H2=12×2+1×2=26
সঠিক উত্তর হবে d) C2H2
2. রাসায়নিক গণনা সংক্ষিপ্ত প্রশ্নোত্তর
রাসায়নিক গণনা সংক্ষিপ্ত প্রশ্নোত্তর
2.1 আণবিক ভর কাকে বলে?
=> H স্কেলে আণবিক ভর- একটি অণু ও একটি হাইড্রোজেন পরমাণুর ভরের অনুপাতকে আণবিক ভর বা আণবিক গুরুত্ব বলে।
আণবিক ভর=\frac{একটি\;অণুর\;ভর}{একটি\;H\;পরমাণুর\;ভর}
অর্থাৎ কোনো অণু একটি H পরমাণুর তুলনায় যতগুন ভারী হয়ে তাকে আণবিক ভর বলে।
12C স্কেলে আণবিক ভর- একটি অণু ও একটি 12C পরমাণুর ভরের 1/12 অংশের অনুপাতকে আণবিক ভর বা আণবিক গুরুত্ব বলে।
আণবিক ভর=\frac{একটি\;অণুর\;ভর}{একটি\;{}^{12}C\;পরমাণুর\;ভর\times\frac{1}{12}}
3. রাসায়নিক গণনা-গাণিতিক প্রশ্ন
3. রাসায়নিক গণনা-গাণিতিক প্রশ্ন
3.1 ফেরাস সালফাইডের সঙ্গে লঘু সালফিউরিক অ্যাসিডের বিক্রিয়ায় 1.7 g হাইড্রোজেন সালফাইড গ্যাস পেতে কত গ্রাম ফেরাস সালফাইড প্রয়োজন হবে? (Fe = 56, S = 32, H = 1 )
=> \underset{\overset{(56 + 32)g = 88g}{?? }}{Fes} + {H}_{2}S{O}_{4}\rightarrow FeS{O}_{4} + \underset{\overset{(1 \times 2 + 32)g = 34g}{1.7g}}{{H}_{2}S}
34 g H2S পেতে প্রয়োজন 88 g H2SO4
1 g H2S পেতে প্রয়োজন \frac{88}{34} g H2SO4
1 g H2S পেতে প্রয়োজন \frac{88\times1.7}{34} g H2SO4
=44 g H2SO4
3.2 জিংক অক্সাইডকে কার্বন সহযোগে উত্তপ্ত করলে ধাতব জিংক ও কার্বন মনোক্সাইড উৎপন্ন হয়। 40.685 গ্রাম জিংক অক্সাইড থেকে 31.785 গ্রাম জিংক ও 14.0 গ্রাম কার্বন মনোক্সাইড উৎপন্ন করতে কত গ্রাম কার্বন প্রয়োজন হবে? বিক্রিয়াটিতে কত মোল কার্বন মনোক্সাইড উৎপন্ন হয়? (C=12, O=16)
=> \underset{40.685g}{ZnO} + C\rightarrow \underset{31.785g}{Zn} + \underset{14g}{CO}
প্রয়োজনীয় কার্বনের পরিমাণ, {(31.785+14)-40.685} g= 5.1 g
1 mol CO = (12+16) g = 28 g
∴ 14 g CO = \frac{14}{28} mol=0.5 mol
3.3 অ্যামোনিয়াম সালফেটকে কস্টিক সোডা দ্রবণসহ উত্তপ্ত করে 6.8 g অ্যামোনিয়া উৎপন্ন করতে কত গ্রাম অ্যামোনিয়াম সালফেট প্রয়োজন হবে? (H = 1, N =14, O = 16, 5 = 32]
=> \underset{?? }{\underset{\{ (14 + 4 \times 1) \times 2 + 32 + 4 \times 16\} g = 132g}{{(N{H}_{4})}_{2}S{O}_{4}}} + 2NaOH\rightarrow {Na}_{2}S{O}_{4} + \underset{6.8g}{\underset{2(14 + 3 \times 1)g = 34g}{2N{H}_{3}}} + 2{H}_{2}O
34 g অ্যামোনিয়া পেতে প্রয়োজনীয় অ্যামোনিয়াম সালফেট = 132 g
1 g অ্যামোনিয়া পেতে প্রয়োজনীয় অ্যামোনিয়াম সালফেট = \frac{132}{34} g
6.8 g অ্যামোনিয়া পেতে প্রয়োজনীয় অ্যামোনিয়াম সালফেট = \frac{132\times6.8}{34} g
=26.4 g
3.4 CaCO3-এর সঙ্গে লঘু HCI-এর বিক্রিয়ায় CaCl2, CO2 ও H2O উৎপন্ন হয়। 50 g CaCO3 থেকে 55.5 g CaCl2, 22.0 g CO2 ও 9.0 g H2O উৎপন্ন করতে কত গ্রাম HCI-এর প্রয়োজন হবে ? প্রয়োজনীয় HCI-এর মোল সংখ্যা কত? (H=1, Cl=35.5)
=> ধরি x g HCl লেগেছে।
বিক্রিয়কের মোট ভর = বিক্রিয়াজাতের মোট ভর
or, CaCO3-এর ভর+ HCl-এর ভর = CaCl2, CO2 ও H2O এর ভর
or, 50+x = 55.5+22+9
∴ x = 55.5+22+9-50 = 36.5
আবার, 1 mol HCl = (1+35.5) g = 36.6 g
36.5 g HCl প্রয়োজন হবে। এর মোল সংখ্যা হল 1
3.5 আয়রন পাইরাইটসকে অতিরিক্ত বায়ুপ্রবাহে পুড়িয়ে সালফিউরিক অ্যাসিডের শিল্পোৎপাদনের জন্য প্রয়োজনীয় SO2 উৎপাদন করা হয়। বিক্রিয়াটির রাসায়নিক সমীকরণ নীচে দেওয়া হল:
4FeS2 + 11O2 → 2Fe2O3 + 8SO2; 512g SO2 উৎপাদনের জন্য কত গ্রাম FeS2 প্রয়োজন ? (Fe = 56, S = 32, O = 16)
=> \underset{4(56 + 32 \times 2) = 480}{4Fe{S}_{2}} + 11S{O}_{2}\rightarrow 2F{e}_{2}{O}_{3} + \underset{8(32 + 16 \times 2) = 512}{8S{O}_{2}}
∴480 g FeS2 প্রয়োজন
3.6 কোনো ধাতব কার্বনেটের 200 g-কে উত্তপ্ত করলে 112 g ধাতব অক্সাইড ও একটি গ্যাসীয় যৌগ উৎপন্ন হয়। গ্যাসীয় যৌগটির বাষ্পঘনত্ব 22। বিক্রিয়াটিতে কত মোল গ্যাসীয় যৌগটি উৎপন্ন হয়?
=> গ্যাসীয় যৌগের ভর- (200-112) g = 88 g। গ্যাসীয় যৌগের আণবিক ভর= 2×22 = 44
∴ মোল সংখ্যা=\frac{88}{44}=2
3.7 উচ্চ তাপমাত্রায় Al দ্বারা Fe2O3 -কে বিজারিত করে 558 g Fe প্রস্তুতির জন্য কত গ্রাম Al প্রয়োজন? বিক্রিয়াটিতে কত মোল Fe2O3 লাগবে? [Fe = 55.8, Al = 27, O = 16]
=> F{e}_{2}{O}_{3} + \underset{??}{\underset{2 \times 27 = 54}{2Al}}\rightarrow A{l}_{2}{O}_{3} + \underset{558}{\underset{2 \times 55.8 = 111.6}{2Fe}}
111.6 g Fe প্রস্তুতির জন্য 54 g Al প্রয়োজন
1 g Fe প্রস্তুতির জন্য \frac{54}{111.6} g Al প্রয়োজন
558 g Fe প্রস্তুতির জন্য \frac{54\times558}{111.6} g Al প্রয়োজন = 270 g Al
আবার,
111.6 g Fe প্রস্তুতির জন্য 1 মোল Fe2O3 প্রয়োজন
1 g Fe প্রস্তুতির জন্য \frac{1}{111.6} মোল Fe2O3 প্রয়োজন
558 g Fe প্রস্তুতির জন্য \frac{1\times558}{111.6} মোল Fe2O3 প্রয়োজন = 5 মোল Fe2O3














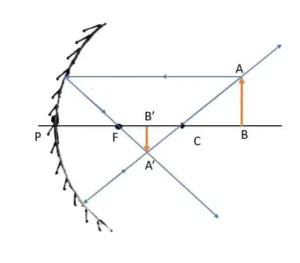



 ABC প্রিজমের প্রতিসারক কোণ ∠A। PQ রশ্মি AC তলে ∠
ABC প্রিজমের প্রতিসারক কোণ ∠A। PQ রশ্মি AC তলে ∠